La malattia coronarica ostruttiva (infarto del miocardio) è un grande incubo per l’umanità. Nei Paesi sviluppati, come la Spagna, è la principale causa di mortalità. Secondo i dati dell’Istituto Nazionale di Statistica, nel 2021 il 26,4% dei decessi era dovuto a malattie cardiovascolari (dati INE).
Il colesterolo alto, soprattutto la frazione LDL (colesterolo cattivo), è indicato come il principale responsabile di questa malattia. L’eccesso di colesterolo LDL nel sangue aumenta la probabilità che si attacchi alle pareti interne dei vasi sanguigni, contribuendo alla formazione di placche di ateroma, aprendo la strada alla cosiddetta aterosclerosi. Di conseguenza, il passaggio si restringe, il flusso sanguigno si riduce e, a seconda della gravità, può esserci il rischio di rottura o blocco del vaso sanguigno. Se ciò avviene nelle arterie del cuore, c’è il rischio di infarto del miocardio (aterosclerosi coronarica).
Per questo motivo, il colesterolo alto è diventato il nemico pubblico numero uno. Paradossalmente, nessuno mette in dubbio che senza colesterolo si muore, e quindi il colesterolo non può essere l’unico colpevole. Infatti, come si spiega il verificarsi di attacchi cardiaci in adulti sempre più giovani, che non presentano anomalie nei livelli di colesterolo e adottano stili di vita apparentemente sani? Sì, c’è un altro colpevole: l’omocisteina.
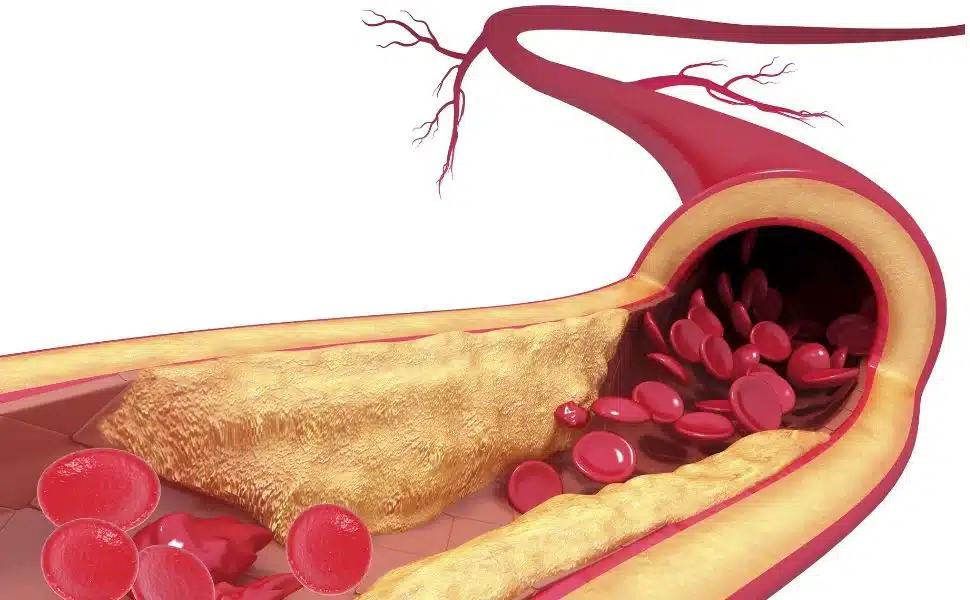
Figura 1: Illustrazione della malattia aterosclerotica (aterosclerosi).
Che cos’è l’omocisteina?
L’omocisteina è un sottoprodotto del metabolismo della metionina, un aminoacido essenziale delle proteine alimentari, soprattutto quelle animali come carne, latte e uova. La metionina viene metabolizzata in omocisteina principalmente nel fegato.
Da dove viene l’omocisteina?
La maggior parte della metionina presente nella dieta viene utilizzata per la sintesi proteica. Tuttavia, una parte significativa viene utilizzata per la formazione di S-adenosil-L-metionina, una molecola di importanza fondamentale in una serie di processi biochimici che coinvolgono la metilazione enzimatica, una reazione biochimica essenziale che svolge un ruolo importante in un’ampia gamma di processi biologici, come l’espressione genica, la sintesi di ormoni, neurotrasmettitori e fosfolipidi.
La metionina si condensa con l’adenosina trifosfato (ATP) nelle cellule, formando la S-adenosil-metionina. Dopo aver donato il gruppo metile, la S-adenosil-metionina viene convertita in S-adenosil-omocisteina, che viene idrolizzata, generando adenosina e omocisteina che vengono rilasciate nel sangue.
L’omocisteina risultante è una molecola molto aggressiva per l’organismo e deve essere metabolizzata (trasformata) in una sostanza meno dannosa. Quando l’omocisteina si trova in livelli elevati nel sangue, noti come iperomocisteinemia, si verificano danni alle pareti interne dei vasi sanguigni, che possono portare all’aterosclerosi attraverso l’accumulo di placche ateromatose e la rigidità arteriosa. 1 Un’altra conseguenza dell’iperomocisteinemia è l’alterazione dei fattori coinvolti nella coagulazione del sangue, che può portare alla formazione di coaguli che innescano la trombosi 1. Alcuni studi hanno anche messo in relazione elevati livelli di omocisteina nel sangue con malattie come l’Alzheimer, il Parkinson, la disfunzione renale e il diabete. 2
Oggi 3, 4, in seguito alla pubblicazione di diversi studi clinici ed epidemiologici, è stato dimostrato che elevati livelli plasmatici di omocisteina sono un fattore di rischio indipendente per l’infarto del miocardio, l’ictus e le malattie vascolari periferiche. È importante notare che un fattore di rischio indipendente significa che è indipendente da altri fattori convenzionali di malattia cardiovascolare, come l’aumento del colesterolo LDL, l’ipertensione o il fumo . Questo è importante, perché se si ha un’omocisteina elevata e un altro fattore di rischio aggiuntivo, la probabilità di malattia cardiovascolare è molto più alta.
Livelli normali di omocisteina nel sangue
Attualmente, le concentrazioni plasmatiche di omocisteina inferiori a 15 µmol/l negli adulti sono considerate non a rischio, mentre i pazienti iperomocisteinemici sono quelli con livelli di omocisteina superiori a questo valore. 6 L’iperomocisteinemia viene solitamente classificata come 7 :
| Classificazione | Concentrazione |
|---|---|
| Lieve | 16 – 30 µmol/L |
| Moderata | 31 – 100 µmol/L |
| Grave | > 100 µmol/L |
Metabolismo dell’omocisteina
Il metabolismo dell’omocisteina nell’organismo avviene principalmente nel fegato, dove intervengono gli enzimi e le vitamine B6 (piridossina), B12 (cobalamina) e il 5-metiltetraidrofolato, generato dal folato (B9). Queste vitamine sono molto importanti perché agiscono come cofattori enzimatici, senza i quali gli enzimi non possono svolgere la loro funzione catalitica.
In che modo le vitamine B6, B12 e B9 sono coinvolte nel metabolismo dell’omocisteina?
Il metabolismo dell’omocisteina avviene attraverso 2 vie principali: la rimetilazione e la trans-sulfurizzazione.
REMETILAZIONE: se l’organismo ha bisogno di metionina, avviene la via della rimetilazione, che coinvolge le vitamine B12 e il 5-metiltetraidrofolato:
TRANSULFURAZIONE: se nell’organismo è presente una quantità sufficiente di metionina, si attiva la via della trans-sulfurizzazione. In questo caso, l’omocisteina si combina irreversibilmente con la serina per generare cistationina. Questa via coinvolge l’enzima cistationina ß sintasi e il suo cofattore vitamina B6. Il passo successivo è la conversione della cistationina in cisteina.
In situazioni normali, l’omocisteina libera nel sangue dovrebbe essere minima. Tuttavia, se i livelli di vitamine B12, B6 e B9 nel fegato sono bassi, il fegato non è in grado di metabolizzare l’omocisteina in modo efficiente, con conseguente iperomocisteinemia, che può portare a gravi problemi di salute, soprattutto a livello vascolare. Infatti, la carenza individuale o combinata di queste 3 vitamine è la causa più comune dell’iperomocisteinemia 6, 8-10.
Va notato che l’iperomocisteinemia può anche essere di origine genetica. L ‘omocistinuria è una malattia genetica che colpisce la funzione degli enzimi coinvolti nel metabolismo dell’omocisteina. Le persone affette da omocistinuria presentano spesso concentrazioni plasmatiche di omocisteina molto elevate, fino a 20 volte superiori ai valori normali. Le manifestazioni cliniche della malattia includono ritardo mentale, dislocazione del cristallino, disturbi scheletrici e arteriosclerosi precoce 11.
L’importanza delle vitamine B6, B12 e dei folati (B9) per il mantenimento di livelli normali di omocisteina.
Nelle persone con livelli elevati di omocisteina, la prima misura terapeutica è una dieta ricca di vitamine B6, B12 e folati. Secondo l’American Heart Association, questa dieta dovrebbe fornire 1,7 mg di vitamina B6, 2,4 µg di vitamina B12 e 400 µg di folato 12 al giorno. Durante la gravidanza o l’allattamento, questo fabbisogno aumenta, così come in alcune malattie come l’insufficienza renale.
Già secondo le conclusioni del Framingham Heart Study, l’apporto giornaliero di vitamina B6 e folati dovrebbe essere rispettivamente di 3 mg e 400 µg di folati per la prevenzione dell’iperomocisteinemia13.
Il Framingham Heart Study è un grande studio di ricerca osservazionale iniziato nel 1948, e tuttora in corso, con l’obiettivo di studiare i fattori di rischio per le malattie cardiovascolari.
I folati nella dieta
Nella popolazione europea, l’assunzione media giornaliera di folati negli uomini e nelle donne è rispettivamente di 291 µg (197-326 µg) e 247 µg/die(168-320 µg). 14 Poiché una percentuale significativa della popolazione non soddisfa il fabbisogno giornaliero di acido folico, una strategia ragionevole per la popolazione consiste nel raccomandare un aumento del consumo di alimenti ricchi di folati. È importante notare che l’acido folico viene facilmente distrutto da un riscaldamento eccessivo e prolungato, che influisce sulla quantità di folato disponibile con la dieta.
Vitamina B12 e veganismo
Nelle persone che seguono una dieta equilibrata, l’apporto di vitamina B12 è di solito adeguato, tranne che nei vegani, che non consumano carne, pesce o latticini. Poiché la vitamina B12 è presente soprattutto negli alimenti di origine animale, i vegani rigorosi possono avere problemi a prevenire l’aumento dell’omocisteina nel sangue. 13
Gastrite atrofica, H. Pylori e vitamina B12
Un altro aspetto importante dell’assorbimento della vitamina B12 è che la vitamina B12 è legata alle proteine presenti negli alimenti. Per rilasciare la vitamina B12 è necessaria l’azione dell’acido cloridrico e degli enzimi presenti nello stomaco. Pertanto, le persone che assumono farmaci per il bruciore di stomaco o il reflusso gastro-esofageo, le persone che soffrono di gastrite atrofica o di infezione da Helicobacter pylori dovrebbero tenere sotto controllo la vitamina B12. Anche l’età spesso porta a una diminuzione della produzione di acido nello stomaco.
Integrazione di supporto
Un’alternativa per garantire l’assunzione di queste vitamine e mantenere livelli normali di omocisteina è l’integrazione. Infatti, diversi studi clinici hanno confermato che l’integrazione di folato (B9), da solo o in combinazione con le vitamine B6 e B12, riduce le concentrazioni plasmatiche di omocisteina per un periodo da 2 a 6 settimane. 13 Questo effetto positivo è stato dimostrato anche in soggetti che non presentavano carenze di nessuna di queste vitamine. Il trattamento con questi integratori vitaminici si è dimostrato efficace, con effetti collaterali minimi e costi contenuti. 13
Magnesio e omocisteina
Sia la metilazione del DNA (a partire dalla S-adenosil-L-metionina) sia la rimetilazione dell’omocisteina in metionina richiedono energia per avvenire. Quando parliamo di energia a livello cellulare, parliamo di ATP (adenosina trifosfato), ed è qui che entra in gioco il magnesio. L’ATP deve essere legato al magnesio per essere biologicamente attivo. In altre parole, ciò che chiamiamo ATP è in realtà ATP-Mg:
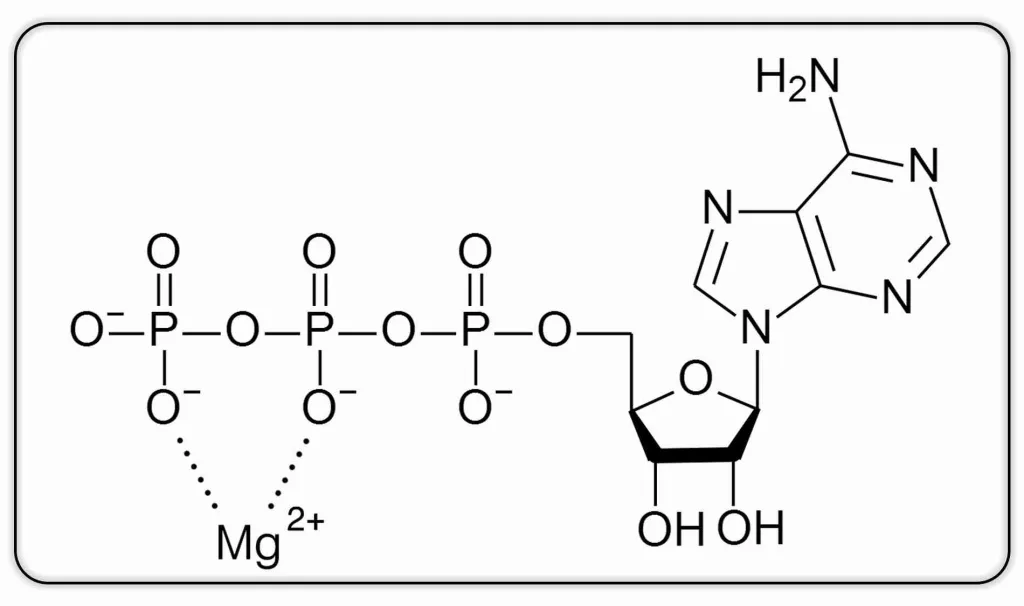
Figura 6: Metabolismo dell’omocisteina – Trans-solfurazione: conversione irreversibile dell’omocisteina in cisteina.
Alcuni ricercatori ipotizzano che il magnesio possa svolgere un ruolo importante nei processi di metilazione, compresa la metilazione del DNA e la rimetilazione dell’omocisteina in metionina. 15 Secondo questi ricercatori, un’inadeguata produzione di ATP-Mg può contribuire all’aumento dei livelli di omocisteina. 15
MAG-FUSION: la fusione del magnesio con le vitamine B6, B9 (folato), B12 e D3
MAG-FUSION è un integratore alimentare a base di Nutribiolite che combina le vitamine B6, B12 e i folati nelle loro forme più bioattive, il magnesio nella sua forma più biodisponibile di citrato di magnesio e la vitamina D3 (colecalciferolo). Si tratta di un integratore alimentare molto completo, ideale per chi ha bisogno di un’integrazione alimentare per controllare i livelli di omocisteina, ma non solo. MAG-FUSION contiene 16:
- Vitamine B6, B9 (folati) e B12 che contribuiscono al normale metabolismo dell’omocisteina e aiutano a ridurre stanchezza e affaticamento.
- Il magnesio e le vitamine B6, B9 (folati) e B12 contribuiscono alla normale funzione psicologica.
- Il magnesio e le vitamine B6 e B12 contribuiscono al normale metabolismo energetico.
- Il magnesio e le vitamine B9 (folati), B12 e D contribuiscono al processo di divisione cellulare.
- Le vitamine B6, B9 (folati), B12 e D contribuiscono al normale funzionamento del sistema immunitario.
- Magnesio e vitamina D che contribuiscono al mantenimento di ossa e denti normali e al normale funzionamento dei muscoli.
- Il magnesio e la vitamina B6 contribuiscono al normale funzionamento del sistema nervoso.
- Il magnesio contribuisce all’equilibrio elettrolitico e alla normale sintesi proteica.
- La vitamina B6 contribuisce alla normale sintesi della cisteina, al normale metabolismo delle proteine e del glicogeno e alla regolazione dell’attività ormonale.
- La vitamina B9 (folati) contribuisce alla normale sintesi degli aminoacidi e alla normale formazione delle cellule del sangue.
- La vitamina D contribuisce al normale assorbimento e utilizzo di calcio e fosforo e al mantenimento di livelli normali di calcio nel sangue.
Nella formula di MAG-FUSION Nutribiolite è stata posta attenzione a selezionare i principi attivi nelle loro forme più bioattive:
Vitamina B6 come pirodoxal-5′-fosfato
La vitamina B6 è un gruppo di tre composti chiamati piridossina, piridossale e piridossamina. Il piridossal-5′-fosfato, noto anche come P5P, è la forma bioattiva della vitamina B6 che può essere utilizzata direttamente dall’organismo senza conversione. Ciascuna di queste forme di vitamina B6 ha funzioni uniche nel nostro organismo, ma solo la forma piridossal-5′-fosfato ha una funzione di cofattore enzimatico, partecipando a circa 168 processi enzimatici vitali nel nostro corpo. 17 Inoltre, la P5P aiuta a trasportare il magnesio attraverso le membrane cellulari, contribuendo ad aumentarne la velocità di assorbimento. 18
Vitamina B12 come metilcobalamina
Esistono due forme di vitamina B12 che è probabile trovare negli integratori alimentari: la metilcobalamina e la cianocobalamina. La cianocobalamina è una forma sintetica di vitamina B12, ampiamente utilizzata negli integratori alimentari perché più economica. Tuttavia, questa forma è meno biodisponibile, poiché l’organismo deve prima liberarsi del gruppo cianuro attraverso l’azione dell’enzima cianocobalamina reduttasi. Dopo l’azione di questo enzima, la cianocobalamina viene infine convertita in metilcobalamina o adenosilcobalamina, che sono le due forme attive della vitamina B12. 19 A differenza della cianocobalamina, la metilcobalamina è una forma naturale di vitamina B12 che può essere ottenuta anche da fonti alimentari come pesce, carne, uova e latte.
Vitamina B9 (folato) come (6S)-5-metiltetraidrofolato (5-MTHF)
Di tutte le forme disponibili di folato, è la forma chimica (6S)-5-metiltetraidrofolato (5-MTHF) quella che ci interessa davvero. Si tratta della forma bioattiva della vitamina B9. Le altre forme devono essere digerite nell’intestino dall’enzima diidrofolato reduttasi (DHFR) per essere convertite in 5-MTHF. 20 Inoltre, il 5-MTHF è presente in MAG-FUSION sotto forma di sale di glucosamina 5-MTHF, noto anche come folato di quarta generazione o Quatrefolic®. Studi di laboratorio hanno dimostrato che questa forma brevettata è 1,8 volte più assorbibile del calcio (6S)-5-metiltetraidrofolato 21, la forma chimica del 5-MTHF utilizzata in altri integratori alimentari. In termini di biodisponibilità, studi in vivo hanno dimostrato che l’assorbimento è 3,1 volte superiore a quello dell’acido folico. 21
I tipi più comuni di omocistinuria sono quelli che colpiscono i geni responsabili della regolazione della produzione degli enzimi CBS e MTHFR. 11 In caso di deficit nella produzione dell’enzima MTHFR, l’organismo non è in grado di produrre 5-metiltetraidrofolato (5-MTHF), la forma bioattiva del folato nell’organismo (Figura 2). Per questo motivo, MAG-FUSION contiene folato direttamente sotto forma di 5-MTHF nella sua formula.
Vitamina D come colecalciferolo (D3)
MAG-FUSION contiene colecalciferolo o vitamina D3 come forma di vitamina D. Questa è la forma più efficace di vitamina D grazie alla sua più efficiente conversione in calcifediolo nell’organismo. L’altra forma di vitamina D è la vitamina D2 o ergocalciferolo. La potenza della vitamina D2 è meno di un terzo di quella della vitamina D3 e la sua azione nell’organismo è più breve .
Magnesio come citrato di magnesio
Il magnesio nella forma chelata del citrato di magnesio, noto anche come citrato di magnesio 3:2, ha un bioassorbimento più elevato (migliore assorbimento da parte dell’organismo) rispetto alle forme chimiche di “sali inorganici” più comunemente utilizzate, come il bicarbonato, il cloruro, l’ossido, il fosfato o il solfato di magnesio. 23, 24
Conclusione
Livelli elevati di omocisteina sono strettamente correlati alla formazione dell’ateroma, la causa principale delle malattie cardiovascolari. Infatti, numerosi studi hanno chiaramente dimostrato che l’iperomocisteinemia è un fattore predisponente per le complicanze ischemiche dell’aterosclerosi, la trombosi venosa e il tromboembolismo polmonare. 25, 26
Data la relazione diretta con lo stato dei folati, della vitamina B12 e della vitamina B6, la prima misura terapeutica è una dieta ricca di queste vitamine. Se non è possibile garantire un apporto giornaliero di 400 µg difolato, 2,4 µg divitamina B12 e 1,7-3 mg di vitamina B6, si raccomanda la supplementazione con integratori alimentari. 27
Se il medico ha confermato che i livelli di omocisteina sono elevati, è bene chiedere se l’integrazione con un integratore alimentare a base di vitamine B6, B12 e folati possa essere utile. In questo caso, consigliamo MAG-FUSION.
- Ganguly, P. e S.F. Alam, Ruolo dell’omocisteina nello sviluppo delle malattie cardiovascolari. Nutr J, 2015. 14: p. 6.
- Sharma, M., M. Tiwari e R.K. Tiwari, Hyperhomocysteinemia: Impact on Neurodegenerative Diseases. Basic Clin Pharmacol Toxicol, 2015. 117(5): p. 287-96.
- Palma Reis, R., Omocisteinemia e malattie vascolari: a che punto siamo nel 2022. Revista Portuguesa de Cardiologia, 2022. 41(10): p. 821-822.
- Porras, A.C., F.B. Vaca e F.G. Sastre, Basi molecolari dell’iperomocisteinemia. Quimica Clinica, 1998. 17(1): p. 5-18.
- Graham, I.M., et al., Plasma homocysteine as a risk factor for vascular disease. Il progetto europeo di azione concertata. Jama, 1997. 277(22): p. 1775-81.
- Varela-Moreiras, G., J.M. Escudero e E. Alonso-Aperte, Omocisteina, vitamine correlate e stili di vita negli anziani: lo studio SÉNECA. Nutrición Hospitalaria, 2007. 22: p. 363-370.
- Morris, A.A., et al., Linee guida per la diagnosi e la gestione del deficit di cistationina beta-sintasi. J Inherit Metab Dis, 2017. 40(1): p. 49-74.
- Heijer, M.d., et al., L ‘integrazione vitaminica riduce i livelli di omocisteina nel sangue. Arteriosclerosi, trombosi e biologia vascolare, 1998. 18(3): p. 356-361.
- Selhub, J., et al., Vitamin Status and Intake as Primary Determinants of Homocysteinemia in an Elderly Population. JAMA, 1993. 270(22): p. 2693-2698.
- Ubbink, J.B., et al., Stato nutrizionale della vitamina B-12, della vitamina B-6 e dei folati in uomini con iperomocisteinemia. Am J Clin Nutr, 1993. 57(1): p. 47-53.
- Przyrembel, H. Omocistinuria. 1982. Berlino, Heidelberg: Springer Berlin Heidelberg.
- Malinow, M.R., A.G. Bostom e R.M. Krauss, Homocyst(e)ine, Diet, and Cardiovascular Diseases. Circulation, 1999. 99(1): p. 178-182.
- McCully, K.S., Omocisteina e malattie vascolari. Nat Med, 1996. 2(4): p. 386-9.
- G, V. e A. E., Ácido fólico y salud, in Fundación Española de la Nutrición. 1999.
- Józefczuk, J., et al., Homocysteine as a Diagnostic and Etiopathogenic Factor in Children with Autism Spectrum Disorder. J Med Food, 2017. 20(8): p. 744-749.
- Regolamento (UE) n. 432/2012 della Commissione, del 16 maggio 2012, che stabilisce un elenco di indicazioni sulla salute autorizzate fornite sui prodotti alimentari, diverse da quelle che si riferiscono alla riduzione del rischio di malattia e allo sviluppo e alla salute dei bambini (aggiornamento del regolamento (CE) n. 1924/2006), in Gazzetta ufficiale dell’Unione europea. 2012.
- Spinneker, A., et al., Stato, carenza e conseguenze della vitamina B6: una panoramica. Nutrizione ospedaliera, 2007. 22: p. 7-24.
- Pouteau, E., et al., Superiorità di magnesio e vitamina B6 rispetto al solo magnesio sullo stress grave in adulti sani con bassa magnesemia: uno studio clinico randomizzato, in singolo cieco. PLOS ONE, 2018. 13(12): p. e0208454.
- Paul, C. e D.M. Brady, Comparative Bioavailability and Utilization of Particular Forms of B(12) Supplements With Potential to Mitigate B(12)-related Genetic Polymorphisms. Medicina integrativa (Encinitas, California), 2017. 16(1): p. 42-49.
- Visentin, M., et al., L’assorbimento intestinale dei folati. Annual review of physiology, 2014. 76: p. 251-274.
- Miraglia, N., et al., Maggiore biodisponibilità orale di un nuovo sale di folato: confronto con l’acido folico e un sale di folato di calcio in uno studio farmacocinetico nei ratti. Minerva Ginecol, 2016. 68(2): p. 99-105.
- Armas, L.A., B.W. Hollis, and R.P. Heaney, Vitamin D2 is much less effective than vitamin D3 in humans. J Clin Endocrinol Metab, 2004. 89(11): p. 5387-91.
- Coudray, C., et al., Studio della biodisponibilità del magnesio da dieci sali organici e inorganici di Mg in ratti impoveriti di Mg utilizzando un approccio con isotopi stabili. Magnesium Research, 2005. 18(4): p. 215-223.
- Kappeler, D., et al., Maggiore biodisponibilità del magnesio citrato rispetto al magnesio ossido dimostrata dalla valutazione dell’escrezione urinaria e dei livelli sierici dopo la somministrazione di una singola dose in uno studio cross-over randomizzato. BMC Nutrition, 2017. 3(1): p. 7.
- Zinellu, A., et al., Una revisione sistematica e una meta-analisi delle concentrazioni di omocisteina nella broncopneumopatia cronica ostruttiva. Clin Exp Med, 2022.
- Chrysant, S.G. e G.S. Chrysant, The current status of homocysteine as a risk factor for cardiovascular disease: a mini review. Expert Rev Cardiovasc Ther, 2018. 16(8): p. 559-565.
- Pintó Sala, X., L ‘omocisteina come fattore di rischio cardiovascolare. Medicina Integrale, 2000. 36(5): p. 179-185.